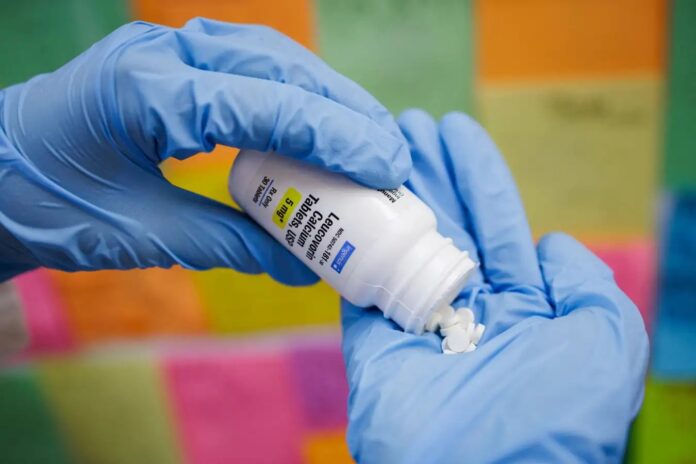
Рішення уряду США прискорити схвалення препарату лейковорин для дітей із церебральним дефіцитом фолієвої кислоти, станом, пов’язаним з аутизмом, викликало суперечки серед медичних працівників. Хоча початкові дані були обмежені невеликими дослідженнями, триває більш масштабне дослідження, результати якого очікуються на початку 2026 року. Це дослідження може дати більш чіткі відповіді щодо потенційних переваг лейковорину для дітей з аутизмом, а також його безпеки.
Контекст: зміна політики та зростання критики
Тиск щодо схвалення лейковорину посилився у 2025 році після суперечливого призначення Роберта Ф. Кеннеді-молодшого очолити медичний заклад Америки. Кеннеді, відомий своїми необґрунтованими заявами проти вакцинації, пообіцяв виявити причини аутизму. Це призвело до рішення уряду прискорити схвалення препарату, незважаючи на скептицизм багатьох експертів. Церебральний дефіцит фолієвої кислоти впливає на засвоєння вітаміну B9, потенційно загострюючи симптоми, схожі на аутизм, такі як проблеми спілкування та сенсорні розлади.
Що говорять наукові дані
Лейковорин вже використовується для інших дефіцитів вітаміну B9 і побічних ефектів лікування раку. Попередні дослідження показують, що він може покращити мову у деяких дітей з аутизмом. Наприклад, дослідження 2016 року показало, що 65% з 23 дітей з аутизмом і порушенням мови показали покращення після 12 тижнів лікування лейковорином, порівняно з 25% у групі плацебо. Однак ці випробування були невеликими, і Міністерство охорони здоров’я та соціальних служб США попереджає, що лейковорин не є ліками.
Випробування 2026: більш масштабне, більш ретельне дослідження
Дослідники під керівництвом Річарда Фрая з медичного центру Rossignol в Арізоні зараз тестують лейковорин у 80 дітей з аутизмом у віці від 2,5 до 5 років. Випробування є найбільшим на сьогоднішній день і має на меті дати більш чітку картину ефективності препарату. Половина дітей отримуватиме лейковорин протягом 12 тижнів, а решта — плацебо, після чого піде друга 12-тижнева фаза, під час якої всі учасники прийматимуть препарат для збору даних про безпеку.
Випробування вимірює зміни в соціальному спілкуванні (як повідомляють батьки), дратівливість, гіперактивність та іншу поведінку, пов’язану з аутизмом. Дослідники також контролюватимуть згортання крові, імунну відповідь і функцію органів, щоб оцінити потенційні побічні ефекти, які наразі погано вивчені у людей з аутизмом.
Залишилися питання та скептицизм
Хоча випробування є кроком вперед, деякі вчені залишаються обережними. Алісія Халладі з Наукового фонду аутизму зазначає, що 80 дітей все одно може бути недостатньо, щоб зробити остаточні висновки, тим більше, що дослідження проводиться лише в одному місці. Механізм, що лежить в основі будь-якої потенційної вигоди, також неясний. Фрай припускає, що препарат може зміцнити зв’язки в мозку, але для підтвердження цього будуть потрібні додаткові сканування.
«Наразі не існує лікування основних симптомів аутизму», — каже Фрай. “Усі ліки, які ми маємо, — це лише пластирі, які лікують симптоми. Це може бути лікування, яке не лише покращує симптоми у цих дітей, але й лікує деякі механізми, що лежать в основі”.
Випробування 2026 року матиме вирішальне значення для визначення того, чи є лейковорин ефективним засобом лікування аутизму чи просто ще одним засобом для лікування симптомів. Результати також прояснить профіль безпеки препарату, який залишається в основному невідомим у цьому контексті.
Результати цього випробування можуть змінити спосіб лікування аутизму, але наразі наукове співтовариство залишається розділеним щодо того, чи є лейковорин реальними перспективами.